2-氰基-3,3-二苯基丙烯酸异辛酯(奥克立林,OCT)是一种广谱紫外线吸收剂,可以吸收长波紫外线(UVA,320~400 nm)和中波紫外线(UVB,280~320 nm),具有很好的防晒效果,因此常常被添加到防晒霜、护肤品等日用品中[1]。但近年来有研究表明OCT会引起光过敏反应和接触性皮炎,且其分子量小,可渗入皮肤,阳光下会释放氧自由基,对皮肤存在潜在危险,增加患皮肤癌几率和加速皮肤细胞衰老[2-5]。为解决上述问题,国内外的研究人员纷纷将视线投向包覆技术,通过将原料包覆,隔离外界环境,从而提高芯材的稳定性,使其缓释、降低刺激性等[6-7],常见的包覆技术包括微胶囊、脂质体、多孔聚合物系统以及凝胶等载体体系[8]。
目前有研究利用脂质体包覆OCT降低其毒性[9-11],但因脂质体与皮肤角质层中的脂类结构相似[12],容易渗入皮肤角质层,不适用于具有潜在致敏、致刺激风险活性物的包覆。微胶囊包覆技术可根据需求选择具有生物相容性的聚合物作为壁材[6, 13],制得的微胶囊具有较好的安全性,同时可以根据需求将微胶囊尺寸降低到纳米尺寸,使其具有更好的分散性和透明性,并能有效减少芯材与皮肤的接触,降低其对皮肤的刺激性[14]。有研究证明将紫外线防护剂包覆形成纳米胶囊能有效增强紫外线的吸收效果[15-17]。
二甲基丙烯酸乙二醇酯(EGDMA)是一种无毒单体,其聚合物聚二甲基丙烯酸乙二醇酯(PEGDMA)是无毒的聚合物,具有良好的生物相容性[18]。本文利用自由基界面聚合法,以EGDMA为单体合成PEGDMA壁材,包裹OCT形成防晒纳米胶囊。为了使OCT具有更好的复配性,在芯材中加入辛酸/葵酸三甘油酯(GTCC),使制得的纳米胶囊具有较小粒径。本文一方面利用PEGDMA包覆OCT/GTCC,降低OCT的毒性,使制得的纳米胶囊具有较好的生物相容性和安全性;另一方面,包覆OCT/GTCC的防晒纳米胶囊具有更好的防晒效果,其SPF值明显提高,在日用化妆品领域具有广泛的应用。
1 实验部分 1.1 原料与试剂EGDMA、过硫酸铵(APS):分析纯,Sigma-Aldrich Co. Ltd;聚乙烯醇(PVA):Mw=3.1×104,醇解度88%,分析纯,Sigma-Aldrich Co. Ltd;OCT:分析纯,TCI;GTCC:工业纯,临沂市兰山区绿森化工有限公司;焦亚硫酸钠(Na2S2O5):分析纯,Adamas Reagent Co. Ltd;甲苯:分析纯,上海凌峰化学试剂有限公司;钙黄绿素:分析纯,上海翊圣生物科技有限公司;Cell Counting Kit-8(CCK-8)试剂盒:上海碧云天生物技术有限公司;磷酸缓冲液(PBS):pH=7.4,美国Hyclone公司;无水乙醇:分析纯,国药集团化学试剂有限公司;小鼠成纤维细胞(L929):细胞株,中国科学院上海细胞库;胎牛血清(FBS):美国Gibco公司;DMEM高糖培养基、双抗(青霉素和链霉素):杭州吉诺生物医药技术有限公司;防晒霜底霜制剂:工业纯,上海上美化妆品有限公司。
1.2 防晒纳米胶囊的制备过程首先,控制总体系质量为50 g,称取7.5 g w=10%的PVA乳化剂溶液置于烧杯中,加入21.3 g去离子水,搅拌均匀作为水相备用。称取15 g芯材(OCT/GTCC)于烧杯中,加入2 g单体EGDMA,搅拌均匀作为油相备用。然后将两相混合后放入冰水浴中,在超声波细胞粉碎机450 W的功率下作用30 min制得O/W纳米预乳液。接着,将预乳液倒入三颈圆底烧瓶后以1 000 r/min速率搅拌,保持温度30 ℃并持续通入氮气,30 min后加入引发剂APS溶液(0.1 g APS溶于2 g蒸馏水),过5 min后加入催化剂Na2S2O5溶液(0.1 g Na2S2O5溶于2 g水),继续通入N2并保持温度不变搅拌3 h。最后将制备得到的纳米胶囊浆液经SD-1500喷雾干燥机干燥制成粉末。
1.3 测试与表征超声波细胞粉碎机:宁波新芝生物科技股份有限公司JY92-IIDN型;实验型喷雾干燥机:上海沃迪自动化装备股份有限公司SD-1500型,进风温度为190 ℃,出风温度为90 ℃,泵的转速为800~1 000 mL/h;台式扫描电子显微镜(SEM):日本日立公司TM-1000型,样品经真空喷金处理;纳米粒度与电位分析仪:英国马尔文仪器公司Nano-ZS,测试前将纳米胶囊乳液适当稀释;透射电子显微镜(TEM):日本JEOL公司JEM-2100型,测试前样品经稀释处理;傅里叶红外光谱仪(FT-IR):美国Thermo Fisher科技公司Nicolet 6700型,扫描范围为4 000~600 cm-1。
采用紫外线透过率分析仪:上海蓝菲(Labsphere)光学仪器有限公司UV-2000S型,利用HelioScreen HD6防晒霜测试基板为载体分别测试样品的SPF值。将一定量的OCT/GTCC和制得的防晒纳米胶囊分别加入底霜制剂中制成防晒霜,并使其中的OCT/GTCC质量分数均为10%。接着称取待测样50 mg滴加在HD6测试基板上,涂抹均匀后称量,使得板上剩余的防晒霜为20~30 mg,静置10 min,待其成膜后用紫外线透过率分析仪测其SPF值。每个基板测5个点,每个待测样测5次取平均值。
采用CCK-8法测试制得的防晒纳米胶囊的生物相容性。首先在96孔板中接种细胞悬液(每孔104个)并在培养箱中37 ℃培养24 h备用;然后将防晒纳米胶囊在紫外光下照射24 h,用磷酸盐缓冲盐水稀释到纳米胶囊的质量浓度10 mg/mL;最后用含有10%牛血清和1%青霉素的培养液将其稀释到不同质量浓度(0, 125, 250, 500, 1 000 μg/mL)与细胞一起培养24 h测定其细胞存活率。为了表征防晒纳米胶囊对芯材的屏蔽作用,将防晒纳米胶囊和芯材分别进行同样的细胞毒性实验,比较其细胞存活率,其中纳米胶囊质量浓度为500 μg/mL,对应芯材的质量浓度通过固含量计算。
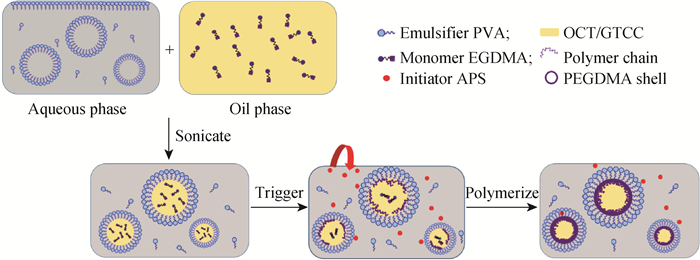
2 结果与讨论 2.1 防晒纳米胶囊的制备过程及机理EGDMA作为单体包覆芯材OCT/GTCC形成防晒纳米胶囊的过程如图 1所示。首先将乳化剂PVA溶于去离子水中形成水相,反应单体EGDMA溶于OCT和GTCC中形成油相,将水相和油相混合,经超声作用形成O/W纳米乳液。然后在30 ℃、N2氛围下,引发剂APS经Na2S2O5催化作用产生初级自由基,在油水界面与单体EGDMA发生作用,使EGDMA活化变成新的自由基并迅速发生自由基聚合反应。最后随着反应的进行,油相中游离的EGDMA会快速移动到油水界面参与反应形成长链高分子自由基。由于EGDMA含有2个双键,长链高分子自由基可发生自交联形成具有三维网状结构的高聚物PEGDMA,并包覆OCT形成纳米胶囊。
|
图 1 制备防晒纳米胶囊的机理图 Fig. 1 Schematic process of preparing NCs |
2.2 防晒纳米胶囊的形貌分析
图 2为纳米胶囊的SEM图。当芯材中不加入GTCC时(图 2(a)),纳米胶囊为不规则的球形,表面不光滑;当芯材中w(GTCC)为10%时(图 2(b)),纳米胶囊为规整的球形,且其表面光滑;当芯材中w(GTCC)为20%时(图 2(c)),纳米胶囊的表面开始凹陷,当w(GTCC)增加到30%时(图 2(d)),纳米胶囊的表面凹陷严重且呈不规则球形。这是由于OCT是油溶性紫外线吸收剂,具有较大的疏水性,加入GTCC使得芯材的疏水性降低,更易被乳化;当芯材中w(GTCC)高于20%时,胶囊开始出现凹陷,这可能是由于过量的GTCC使芯材黏度变小,乳化体系的稳定性降低,芯材不易被包覆[19]。因此,当芯材中w(GTCC)=10%时,所制得的球形防晒纳米胶囊形貌最为规整,后文的实验在此基础上进行研究。

|
图 2 纳米胶囊的SEM图 Fig. 2 SEM images of NCs |
2.3 防晒纳米胶囊的粒径分布及其核-壳结构
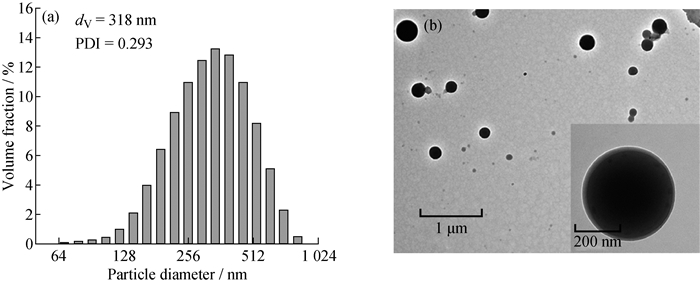
图 3为防晒纳米胶囊的粒径分布图(图 3(a))和TEM图(图 3(b)),由图 3(a)可知,制得的防晒纳米胶囊的平均粒径(dV)为318 nm,PDI为0.293,属于微纳米范围,能减少进入皮肤的风险[15]。由图 3(b)可知,防晒纳米胶囊为规整的球形,表面光滑致密,具有明显的核-壳结构,壁厚为20~25 nm,说明芯材OCT/GTCC已被成功包覆于壁材中。
|
图 3 防晒纳米胶囊的粒径分布图(a)和TEM图(b) Fig. 3 Particle size distribution (a) and transmission electron micrograph (b) of NCs |
2.4 防晒纳米胶囊的组分分析
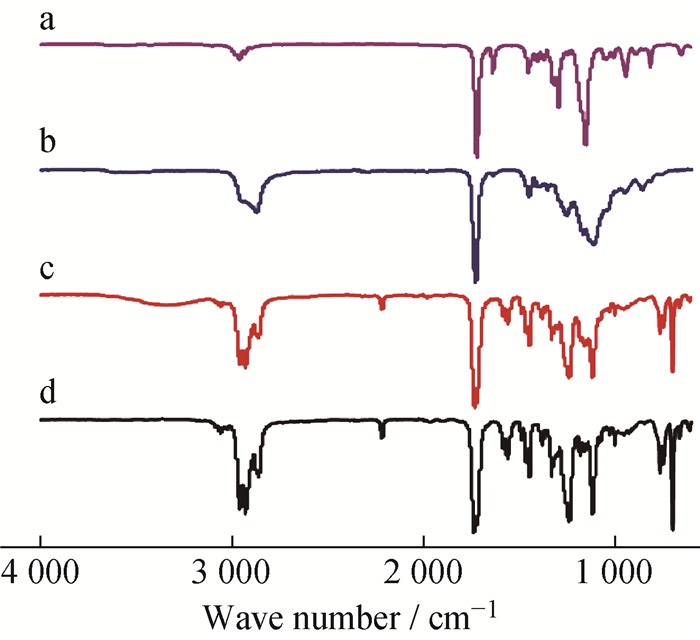
图 4为样品的FT-IR谱图。由图 4可知,单体EGDMA在1 638 cm-1和943 cm-1处的特征吸收峰为—C═C(CH3)—的伸缩振动峰; 而在防晒纳米胶囊中,C═C双键对应的吸收峰大部分已经消失,说明单体EGDMA在自由基界面聚合形成胶囊时,几乎完全反应形成壁材,在1 733、2 217、3 059、1 559 cm-1处的吸收峰分别对应—C═O酯基的伸缩振动、—C≡N的伸缩振动、苯环C—H的伸缩振动以及苯环的骨架振动。通过与壁材PEGDMA和芯材OCT/GTCC的吸收光谱比较,纳米胶囊红外光谱的吸收峰包含了两者所有特征吸收峰,并且无其他新的特征吸收峰出现,也未曾减少原有的吸收峰,说明芯材和壁材没有发生化学反应,并且PEGDMA已成功包覆OCT/GTCC形成防晒纳米胶囊。
|
a—EGDMA; b—PEGDMA shell; c—NCs; d—OCT/GTCC 图 4 样品的红外吸收光谱图 Fig. 4 FT-IR spectra of samples |
2.5 防晒纳米胶囊的防晒性能分析
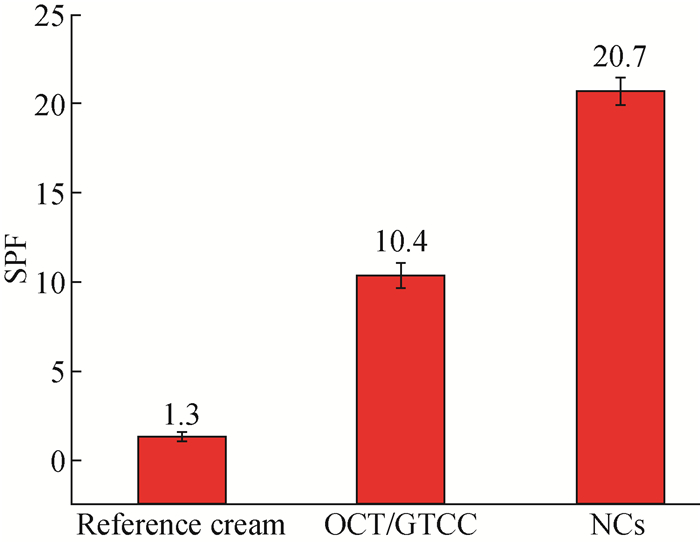
将芯材OCT/GTCC和防晒纳米胶囊分别添加到底霜制剂中制成防晒霜,使OCT/GTCC的质量分数均为10%。利用紫外线透过率分析仪测试其SPF值。如图 5所示,纳米胶囊化的OCT,其SPF值比未包覆之前提高了99%,其防晒功能明显增强。主要原因是壁材PEGDMA是透明的,紫外线照射到纳米胶囊壁材表面发生反射、散射和折射等物理作用,经反射和散射后的紫外线可能进入空气,也可能与其他纳米胶囊继续发生作用;而经折射进入纳米胶囊内部的紫外线将被紫外线吸收剂OCT吸收。因此在物理反射、散射、折射和化学吸收等复杂作用下,紫外线的伤害作用被明显降低,说明该防晒纳米胶囊具有更强的防晒功能,同时SPF值明显提高[20]。
|
图 5 底霜、含OCT/GTCC的防晒霜以及含防晒纳米胶囊的防晒霜的SPF值 Fig. 5 SPF of reference cream and creams based on OCT/GTCC and NCs |
2.6 防晒纳米胶囊的生物相容性分析
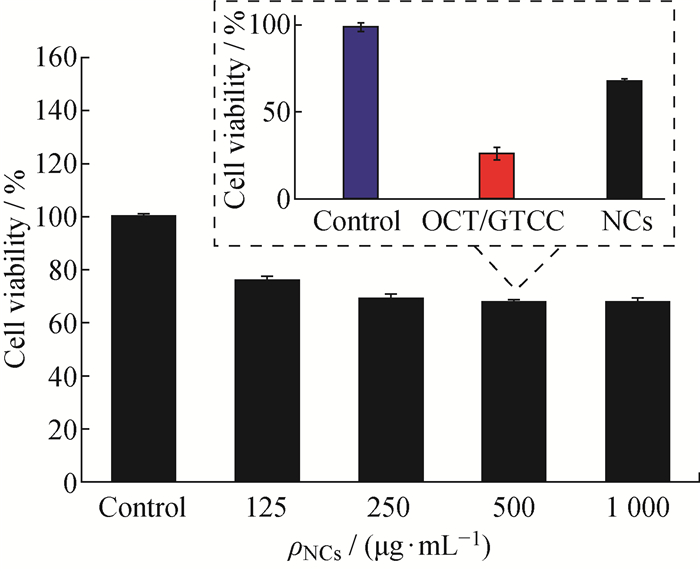
为了测定防晒纳米胶囊的安全性和生物相容性,对其进行细胞毒性试验,结果如图 6所示。不同质量浓度(125~1 000 μg/mL)的防晒纳米微胶囊与细胞培养24 h后,细胞的存活率约为70%或大于70%,且随着纳米胶囊质量浓度的增加,细胞存活率并没有明显下降,说明制得的防晒纳米胶囊具有良好的生物相容性。导致细胞存活率下降的原因可能是防晒纳米胶囊的壁上附着有游离的OCT。将500 μg/mL的防晒纳米微胶囊和未包覆芯材分别与细胞培养,结果如图 6插图所示,与防晒纳米胶囊相比,未包覆的芯材使细胞的存活率大大降低,说明防晒纳米胶囊能明显降低芯材对细胞的毒性。综上证明,将芯材OCT/GTCC包覆形成纳米胶囊,能明显降低芯材的毒性作用,且制得的纳米胶囊具有良好的生物相容性和安全性。
|
图 6 纳米胶囊与细胞培养24 h后的细胞存活率(插图:500 μg/mL的纳米胶囊和OCT/GTCC分别与细胞培养24 h后的细胞存活率) Fig. 6 Cell viability of cells incubated with NCs for 24 h (Insert: cell viability of cells incubated with OCT/GTCC and NCs for 24 h (ρ=500 μg/mL)) |
3 结论
(1) 以EGDMA为单体成功包覆OCT和GTCC制备得到防晒纳米胶囊,该纳米胶囊呈光滑的球形,平均粒径为318 nm,PDI为0.293,具有良好的分散稳定性。
(2) 将紫外线吸收剂OCT包覆后,制得的防晒纳米胶囊具有更高的SPF值,即纳米胶囊具有更好的防晒性能。
(3) 该纳米胶囊具有良好的生物相容性,能明显降低OCT的毒性,为皮肤提供更持久的保护作用。
| [1] | ISABELLA K, KATRIEN V B, JERKER M, et al. Clinical and experimental studies of octocrylene's allergenic potency[J]. Contact Dermatitis, 2011, 64(6): 343–352. DOI:10.1111/cod.2011.64.issue-6 |
| [2] | MANOV E, VON G N, HUNGERB HLER K. Ultraviolet filter contact and photocontact allergy:Consumer exposure and risk assessment for octocrylene from personal care products and sunscreens[J]. Br J Dermatol, 2014, 171(6): 1368–1374. DOI:10.1111/bjd.13372 |
| [3] | AVENEL-AUDRAN M, DUTARTRE H, GOOSSENS A, et al. Octocrylene, an emerging photoallergen[J]. Arch Dermatol, 2010, 146(7): 753–757. |
| [4] | de GROOT A C, ROBERTS D W. Contact and photocontact allergy to octocrylene:A review[J]. Contact Dermatitis, 2014, 70(4): 193–204. DOI:10.1111/cod.12205 |
| [5] | 李建, 陈庆生, 孙永, 等. 一种微囊包裹化学型紫外吸收剂技术研究[J]. 日用化学品科学, 2014, 37(5): 24–27. |
| [6] | 罗绍强, 张晨, 牛玉莲, 等. 包覆技术及其在化妆品中的应用现状[J]. 日用化学工业, 2015, 45(3): 169–174. |
| [7] | BLASI P, SCHOUBBEN A, GIOVAGNOLI S, et al. The real value of novel particulate carriers for sunscreen formulation[J]. Expert Review of Dermatology, 2014, 6(5): 509–517. |
| [8] | 强正. 化妆品防晒剂包覆技术的研究进展[J]. 香料香精化妆品, 2010(3): 43–45. |
| [9] | POPA A, NICULAE G, MEGHEA A. Co-encapsulation of a mixture of antioxidant and sunscreen agents into solid lipid nanoparticles[J]. Upb Scientific Bulletin, 2014, 76(2): 45–56. |
| [10] | NICULAE G, BADEA N, MEGHEA A, et al. Coencapsulation of butyl-methoxydibenzoylmethane and octocrylene into lipid nanocarriers:UV performance, photostability and in vitro release[J]. Photochem Photobiol, 2013, 89(5): 1085–1094. DOI:10.1111/php.2013.89.issue-5 |
| [11] | LACATUSU I, BADEA N, MURARIU A, et al. The encapsulation effect of UV molecular absorbers into biocompatible lipid nanoparticles[J]. Nanoscale Research Letters, 2011, 6(1): 73–81. DOI:10.1186/1556-276X-6-73 |
| [12] | 张宏利. 微胶囊化妆品与脂质体化妆品[J]. 辽东学院学报(自然科学版), 2002, 9(1): 21–22. |
| [13] | 林书乐, 王坤. 微胶囊技术新进展[J]. 高分子材料科学与工程, 2012, 28(5): 179–182. |
| [14] | 叶琳, 肖作兵. 纳米微胶囊技术与纳米化妆品研究进展[J]. 香料香精化妆品, 2006(4): 22–26. |
| [15] | BLUME G, JUNG K. New nanocapsules with high loading of UV-filters[J]. Sofw Journal, 2010, 136: 50–55. |
| [16] | ROTTMAN C, GANS O, BIAGINI F, et al. Advanced sunscreens:UV absorbers entrapped in sol-gel glass microcapsules[J]. J Sol-Gel Sci Technol, 2002, 23(3): 268–270. DOI:10.1023/A:1013987201086 |
| [17] | KAPUAŚCIŃSKA A, OLEJNIK A, NOWAK I. Chapter 8-nanocapsules as carriers of active substances[J]. Nanobiomaterials in Galenic Formulations and Cosmetics, 2016, 10: 175–199. |
| [18] | 焦鑫, 赵迪, 张姚, 等. 聚二甲基丙烯酸乙二醇酯壁材微胶囊的制备及其表征[J]. 高分子学报, 2016(3): 345–351. DOI:10.11777/j.issn1000-3304.2016.15215 |
| [19] | JIAO X, ZHAO D, ZHANG Y, et al. Synthesis and studies of poly(ethylene glycol dimethacrylate) microcapsule[J]. Colloid Polym Sci, 2016, 294(4): 639–646. DOI:10.1007/s00396-015-3815-1 |
| [20] | SHI L, SHAN J, JU Y, et al. Nanoparticles as delivery vehicles for sunscreen agents[J]. Colloids and Surfaces A:Physicochemical and Engineering Aspects, 2012, 396: 122–129. |
 2018, Vol. 31
2018, Vol. 31


