pH敏感化合物是指在固态或溶液状态下,通过改变结构或性能的方式,响应体系的pH发生变化的变色化合物[1]。大部分酸致变色化合物在结构上都存在胺基(-NH2)[2]或希夫碱结构(-C=N-)[3]。酸致变色化合物与低浓度酸作用时,这些基团接收质子并改变化合物的分子结构或堆积方式,从而导致其紫外可见光谱或荧光光谱的明显变化。因此,酸致变色化合物的制备和性能研究在pH传感器、光或化学开关以及气体控制的可逆变色装置等领域具有重要的应用前景[4]。
从分子结构上可将酸致变色化合物分为小分子[2-5]、非共轭高分子[6-10]和共轭高分子[1, 11-13]三种。虽然小分子或非共轭高分子在酸致变色方面表现良好,但其结构中的质子敏感单元与质子作用后,只引起分子结构的局部变化,从而导致这类化合物的酸致变色灵敏度较低。结构中含有质子敏感单元(-NH2或-C=N-)的共轭高分子可以弥补该缺陷。组成共轭高分子的每一个单元中,参与共轭的原子通过离域的大π电子相互关联,一旦某个单元中的一个氮原子和质子作用,就会引起整体分子共轭程度的变化,最终表现在共轭分子性能的变化上。因此,为了提高酸致变色化合物的灵敏度,研究者开始关注结构中含有希夫碱结构(-C=N-)或胺基(-NH2)的共轭高分子化合物的酸致变色性能研究[1, 11-13]。研究结果显示,这类共轭高分子紫外可见光光谱和荧光光谱对低浓度质子变化有良好的敏感性。本课题组在研究含喹喔啉的电子给体-电子受体-电子给体(D-A-D)型共轭聚合物时观察到,以烷基噻吩为电子给体的含喹喔啉共聚物溶液与低浓度质子酸作用时,其紫外可见光光谱和荧光光谱发生了较大的变化[14]。适当地改变电子给体单元的结构可调控该类型聚合物的紫外可见光光谱和荧光光谱,使其具有更好的酸致变色性能,提高其在pH敏感荧光探针开发中的应用价值。
芴因具有刚性的平面内联苯结构,其高聚物和低分子衍生物在固态时具有较高的荧光量子产率,在分子结构中引入芴可有效提高或赋予目标产物良好的荧光性能[15-18]。因此,本文以单喹喔啉为缺电子单元、烷基芴为富电子单元,制备了4种D-A结构的共轭聚合物,讨论了单体和聚合物的结构,以及聚合物的溶液与低浓度质子酸作用时的紫外可见光光谱和荧光光谱。
1 实验部分 1.1 主要试剂与原料丁基锂正己烷溶液(LB,2.5 mol/L)、1-溴正辛烷(OB)、溴素(BROMINE)、三氟乙酸(TFA)、异丙醇频哪醇硼酸酯(PPB)、二氯化钯(PC):分析纯,上海阿拉丁生化科技股份有限公司;4, 7-二溴-2, 1, 3-苯并噻二唑(DBBTA)、芴(FLUORENE)、邻菲罗啉(PT)、联苯甲酰(BENZIL)、菲醌(PTQ)、苊醌(ATQ)、无水三氯化铁(AHFC):分析纯,上海大瑞精细化工公司;氘代氯仿:优级纯,上海波卡试剂公司;参照文献合成5, 6二酮-1, 10-邻菲罗啉(DPT)[19]、2, 7-二(4, 4, 5, 5-四甲基-1, 3, 2-二氧杂硼酸烷)-9, 9-二辛基芴[20](单体M5)。
在氮气保护下向四氢呋喃(THF)中加入金属钠,以回流的方式去水,准备无水反应所需的溶剂,二苯甲酮作为无水显色剂,无水标准是溶剂颜色变紫蓝色,使用时现蒸现用。
1.2 单体的合成
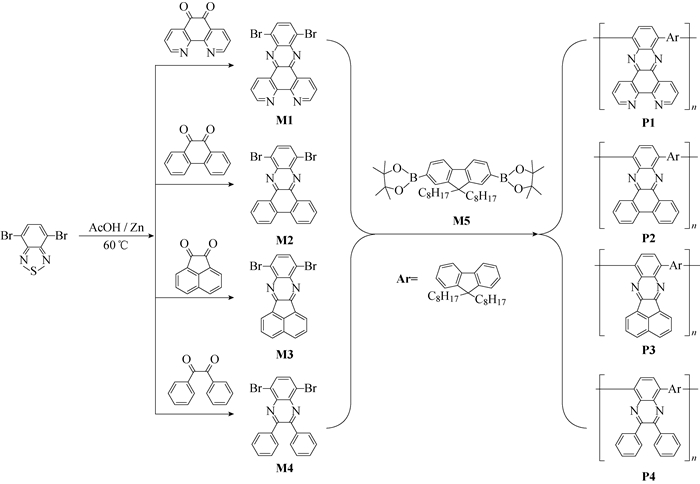
|
图 1 单体和聚合物的合成路线 Fig. 1 Schematic synthesis routes for monomers and polymers |
单体M1亮黄色固体,产率为64%。1H-NMR (400 MHz, CDCl3) : 9.75~9.73(d, J=8.0 Hz, 2H); 9.34~9.32(d, J=8.0 Hz, 2H); 8.11(s, 2H); 7.88~7.85(m, 2H)。UV-Vis(nm):366,385。
单体M2淡黄色固体,产率71%。1H-NMR (400 MHz, CDCl3) : 9.49~9.47(d, J=8.0 Hz, 2H); 8.59~8.57(d, J=8.0 Hz, 2H); 8.03(s, 2H); 7.87~7.77(m, 4H)。UV-Vis(nm):382,403。
单体M3为苍黄色固体,产率68%。1H-NMR (400 MHz, CDCl3) : 8.58~8.56(d, J=8.0 Hz, 2H); 8.19~8.17(d, J=8.0 Hz, 2H); 7.93(s, 2H); 7.91~7.87(t, 2H)。UV-Vis(nm):312,322,369。
单体M4为苍黄色固体,产率76%。1H-NMR (400 MHz, CDCl3) : 7.92(s, 2H); 7.67~7.64(m, 4H); 7.43~7.34(m, 6H)。UV-Vis(nm):357。
1.3 聚合物的合成以聚合物P1为例:将单体M1(300 mg, 0.681 6 mmol)和单体M5(479 mg, 0.681 6 mmol)置于250 mL的双口圆底烧瓶中,加入甲苯(100 mL)和K2CO3溶液(12 mL, w=20%),随后抽真空并充N2置换反应体系的空气,之后加入催化剂Pd(CH3COO)2(30 mg, 0.136 3 mmol)和配体三环己基膦(114 mg, 0.409 0 mmol),室温搅拌2 h后,升温回流反应72 h。反应结束后,减压蒸出有机溶剂,将剩余物溶解于CH2Cl2(300 mL)并分别用稀盐酸(100 mL, w=10%)和氨水(100 mL)洗涤,每次室温搅拌12 h。分出有机相并用盐水洗涤数次后,用无水MgSO4干燥。减压蒸馏蒸出有机溶剂,乙醇重结晶得黄棕色产物342 mg,产率为69%。1H-NMR (400 MHz, CD3Cl): 9.83 (s, 2H); 9.51 (m, 2H); 8.43~8.40 (m, 2H); 8.29~7.54 (m, 8H); 6.96~6.78(m, 2H); 2.98~2.41 (m, 4H); 2.27~1.78 (m, 4H); 1.43~0.64 (m, 26H)。UV-Vis(nm):452。
聚合物P2、P3、P4的制备方法同P1, 其合成路线如图 1所示。
P2为橙黄色固体,产率为72%。1H-NMR (400 MHz, CDCl3): 9.33~9.16 (m, 2H); 8.67~8.51 (m, 2H); 8.27~7.59 (m, 14H); 2.37~2.15 (m, 4H); 1.36~0.99 (m, 24H); 0.88~0.65 (m, 6H)。UV-Vis(nm):439。
P3为黄绿色固体,产率45%。1H-NMR (400 MHz, CDCl3): 8.20~7.81 (m, 8H); 7.75~7.58 (m, 4H); 7.41~7.28 (m, 4H); 2.30~2.08(m, 4H); 1.37~1.01 (m, 24H); 0.90~0.67 (m, 6H)。UV-Vis(nm):412。
P4为黄绿色固体,产率48%。1H-NMR (400 MHz, CDCl3): 8.71~7.49 (m, 18H); 2.37~1.96(m, 4H); 1.78~1.41 (m, 4H); 1.37~1.02 (m, 20H); 0.87~0.61 (m, 6H)。UV-Vis(nm):416。
1.4 表征1H-NMR核磁共振:美国VARIANINOVA-400 MHz型核磁共振仪(TMS为内标,P1~P4均溶解在CDCl3中);紫外-可见(UV-Vis)分光光度计:日本Shimadzu UV-2550型(P1~P4均溶解在CHCl3中;P1、P2、P3、P4的质量浓度依次为25.0、80.0、70.0、30.0 mg/L);荧光光谱仪:日本岛津(P1~P4均溶解在CHCl3中;P1、P2、P3、P4的质量浓度依次为11.0、32.0、28.0、10.0 μg/L)。
2 结果与讨论 2.1 聚合物的表征图 2是聚合物P1和单体M1、M5的红外光谱对比图(图 2(a))以及聚合物P1~P4的红外光谱图(图 2(b))。从图 2(a)中可知,在单体M5的红外谱图中,2 979~2 952 cm-1处的峰归属于芳香环上C-H的伸缩振动;2 927~2 852 cm-1处的峰归属于饱和脂肪链上的C-H伸缩振动;1 350 cm-1处的强振动峰属于B-O键和CH3的振动的缔合, 1 142 cm-1处可能与B-C振动有关,828 cm-1处为(CH2)n的振动峰。在单体M1的红外谱图中,3 065、3 021、2 959 cm-1处出现喹喔啉型单体结构中芳香环上C-H的伸缩振动峰,1 585、1 570、811、741 cm-1处的峰归属于喹喔啉结构中(包括吡啶环) -C=N-的振动;1 477、1 454、1 442 cm-1处的峰归属于芳香环上C=C的伸缩振动;988、899 cm-1处的峰归属于C-Br的伸缩振动。聚合物P1的红外谱图中,3 063、3 025 cm-1处出现了喹喔啉型单体结构中芳香环上C-H的伸缩振动峰,2 923、2 851 cm-1处出现了饱和脂肪链上CH3和CH2的C-H伸缩振动峰;1 656、1 607、1 579、811、741 cm-1处出现喹喔啉结构中吡啶环上的CN-的振动峰,与单体M1相比增加了1 656、1 607 cm-1处的2个振动峰;芳香环上C=C的伸缩振动峰蓝移至1 489、1 458 cm-1;单体M5在1 350 cm-1处的B-O振动峰和单体M1在987、897 cm-1处的C-Br振动峰消失;与单体相比,1 700~400 cm-1处的吸收峰在聚合物谱图中发生重叠并变宽[1],这些变化可能是因为2种单体在催化剂的作用下发生聚合所引起的,因此初步确定聚合物合成成功,其余聚合物的红外谱图特征峰的变化情况类似于P1。
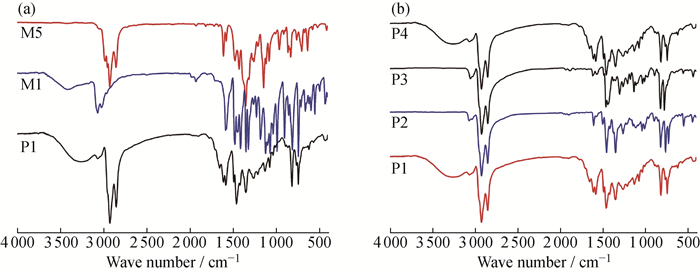
|
图 2 样品的FT-IR光谱 Fig. 2 FT-IR spectra of samples |
图 3是聚合物P1~P4的1H-NMR谱图,以聚合物P1的1H-NMR谱图为例讨论聚合物的表征结果。在氘代氯仿中,化学位移在9.83处的信号峰对应吡啶环氮原子邻位的质子;9.51处的信号峰对应吡啶环氮原子对位的质子;8.42处的信号峰对应喹喔啉苯环上的质子;8.29~7.54处的信号峰对应芴结构中的质子;3.0~0.5处的信号峰对应二辛基芴结构上烷基的质子。在单体M5中,与4, 4, 5, 5-四甲基-1, 2, 3-二氧杂硼烷有关的质子化学位移在聚合物的核磁共振氢谱图中消失了,单体M5中的芴结构上的质子化学位移在聚合物核磁共振氢谱图中向低场移动,且这几个质子的化学位移重叠合并,说明喹喔啉结构和烷基芴结构通过Suzuki反应交联形成了聚合物P1。
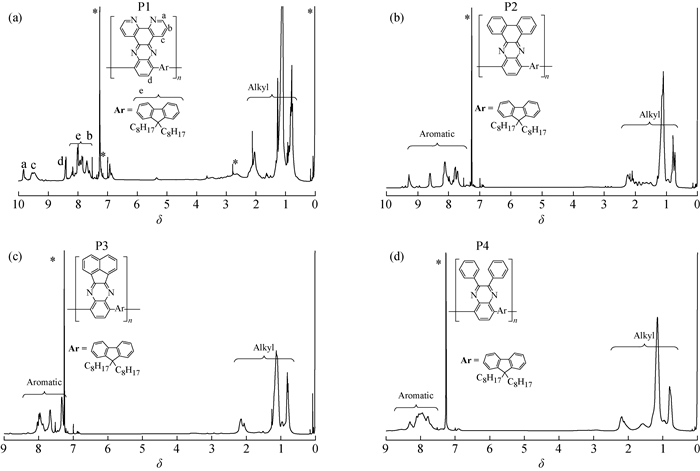
|
图 3 聚合物的核磁共振氢谱图 Fig. 3 1H-NMR spectra of polymers |
2.2 聚合物的紫外-可见光光谱分析及其酸致变色性能
图 4是聚合物P1~P4的CHCl3溶液在本征态以及加入低浓度TFA时的UV-Vis光谱图。酸致变色前后的对比图见图 5。
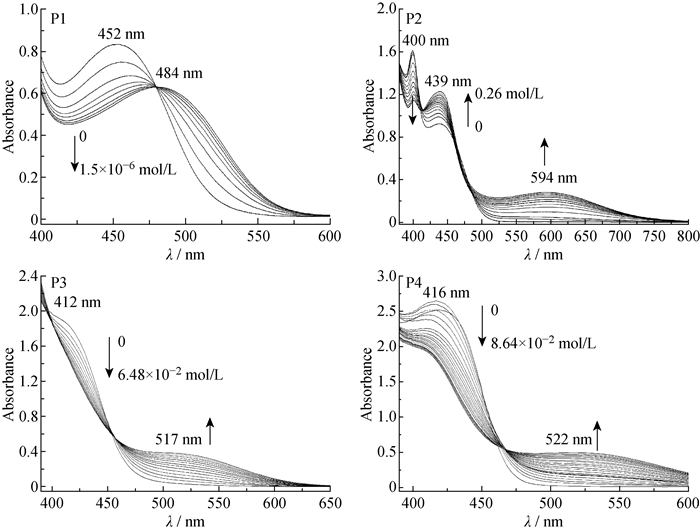
|
c(TFA) is increased stepwise and the increase amount in each step is 2.17×10-7 mol/L for P1, 2.16×10-2 mol/L for P2, 4.32×10-3 mol/L for P3 and P4 图 4 聚合物的本征态和加入不同浓度TFA时的UV-Vis光谱图 Fig. 4 UV-Vis spectra of polymers at neutral state and after added TFA acid |

|
图 5 P1~P4溶液加入TFA前后的颜色变化 Fig. 5 Colour changes of the P1-P4 solution before and after added TFA |
由图 4可知,P1的本征态在400~600 nm存在一个吸收带,最大吸收峰出现在452 nm。加入TFA后,P1在452 nm处吸收峰的吸光值下降并发生红移。随着TFA浓度的增加,聚合物的吸收峰吸光值继续下降并保持红移。当TFA浓度增加到1.5×10-6 mol/L时,聚合物在452 nm处的吸收峰红移32 nm,出现在484 nm处。这是因为溶液中加入TFA时,聚合物P1结构中的喹喔啉单元上吡啶环的两个C=N结构与质子结合,这时C=N结构带正电荷,与溶液中的三氟乙酸根负离子作用,在聚合物分子链周围形成双电层。因三氟乙酸根体积较大,聚合物分子链在三氟乙酸根作用下发生扭转使结构中各单元共平面性增加。随着TFA浓度增加,聚合物分子链中吡啶环上更多的C=N结构与质子结合,增加了聚合物分子链的扭转程度,最终导致聚合物分子链总体共轭程度增加,吸收峰发生更多的红移。在以前的研究中观察到[1, 14],结构中含喹喔啉单元的聚合物与TFA作用时,质子进入喹喔啉单元中的C=N结构上,使聚合物分子链发生较大程度的扭转,这时聚合物的共轭程度增加,导致原先的吸收峰吸光值变小,并在长波长处出现新吸收带。但是,本文中的聚合物P1与TFA作用时没有出现这种变化,只是原有的吸收带吸光值变小且发生了小幅度红移。聚合物P1的CHCl3溶液与0.1 mol/L的TFA作用得到的结果与1.5×10-6 mol/L时的结果一样。这是因为,聚合物P1的喹喔啉单元中存在2个吡啶环,而且吡啶环在喹喔啉单元的最外层,空间阻力很小,很容易与质子作用。因此,与聚合物P2~P4相比,P1能和很低浓度的TFA作用,其喹喔啉单元中的2个吡啶环一旦与TFA作用将形成正电荷,可降低喹喔啉单元的总体电荷密度,导致喹喔啉结构中的C=N很难与TFA作用。因此,P1对很低浓度的TFA敏感。在此过程中,聚合物P1的CHCl3溶液颜色从本征态的橙黄色变成橙红色。
P2的本征态在380~800 nm处存在2个吸收带,最大吸收峰出现在400 nm和439 nm处。随着TFA浓度增加,P2在400 nm处的吸光值下降,在439 nm处的吸光值上升,同时在500~800 nm出现新的宽吸收带。当TFA浓度增加到0.26 mol/L时,500~800 nm的最大吸收峰出现在594 nm处。引起这种变化的原因在聚合物P1的谱图分析和文献[1, 14]中做了详细讨论。从聚合物P2与TFA作用后的结果可知,在400 nm处的吸收带是由聚合物喹喔啉单元结构产生的,而在439 nm和594 nm处的吸收带是由共轭聚合物分子链产生的,因此聚合物分子链共轭程度的增加导致这些吸收带的吸光值变大。聚合物P3、P4本征态溶液的酸致变色性能类似于聚合物P2。
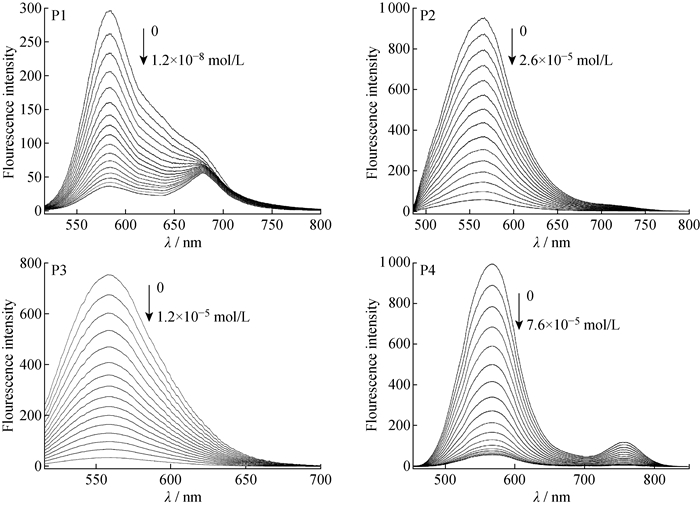
2.3 聚合物的荧光光谱图图 6为P1~P4的CHCl3溶液本征态和加入不同浓度的TFA时的荧光光谱图,聚合物的激发波长和发射波长数据见表 1。由图 6可知,聚合物溶液中加入低浓度TFA时,荧光强度显著减弱,并随着TFA浓度的增加荧光强度继续减弱。当TFA加入量达到各自极限值时,荧光强度几乎为零。引起荧光光谱变化的原因是:当溶液中加入TFA时,聚合物发生掺杂,即喹喔啉单元中C=N结构与质子作用,使喹喔啉结构带正电荷。这种质子化作用一方面可改变吸光发光过程中的非辐射能量转移,另一方面喹喔啉单元质子化后,聚合物分子单元上的正电荷和溶液中的三氟乙酸根负离子相互作用,迫使聚合物分子链发生扭转,进一步增加了聚合物分子的共轭程度及分子内部的光电子转移。以分子链发生扭转后形成的“扭转的分子内电荷转移态”作为新的荧光发射态,可改变荧光激发所需的波长。此外上述2个因素可增加分子内和分子间的无辐射能量转移,从而最终导致荧光强度的减弱[1]。
|
c(TFA) is increased stepwise and the increase amount in each step is 7.0×10-10 mol/L for P1, 1.73×10-6 mol/L for P2, 7.5×10-7 mol/L for P3 and 4.0×10-6 mol/L for P4 图 6 聚合物本征态和加入不同浓度TFA时的荧光光谱图 Fig. 6 Fluorescence spectra of polymers at neutral state and after added TFA acid |
|
|
表 1 聚合物的激发和发射波长 Table 1 Excitation and emission wavelength of polymers |
总之,当溶液中加入TFA后,聚合物分子链结构、分子轨道和能级发生了变化,最终导致荧光淬灭。此外,P1溶液对7.0×10-10 mol/L的TFA敏感,而P2~P4溶液分别对1.73×10-6、7.5×10-7、4.0×10-6 mol/L的TFA敏感。这是因为P1的喹喔啉单元结构中有2个吡啶环,吡啶环周围的空间阻力很低,很容易与质子作用,而P2~P4的喹喔啉结构与质子作用时,质子必须进入到喹喔啉环,喹喔啉环周围的空间阻力很大,因此质子进入喹喔啉环所需要的浓度较大。
从图 6可知,聚合物P1的荧光光谱强度较小,而P2~P4的荧光强度较大。这可能是因为P1的喹喔啉结构中存在2个吡啶环,增加了其分子极性,从而使分子间作用力变大,分子容易堆积,分子间无辐射能量转移增加,即产生了一种高分子效应。相反,P2~P4的分子极性相对较小,溶液中分子间距离较大,分子间能量转移较低,因此荧光强度相对较大。
3 结论(1) 以DBBTA为原料,通过还原获得二胺基中间体,并分别与DPT、PTQ、ATQ和BENZIL缩合反应,制备了4种单喹喔啉衍生物。
(2) 在Pd(CH3COO)2催化下,单喹喔啉衍生物与二辛基芴通过Sukuzi反应交替共聚制备了聚合物。
(3) P1~P4的CHCl3溶液的UV-Vis光谱和荧光光谱对低浓度TFA具有良好的敏感性,其中喹喔啉单元结构中有2个吡啶环的P1与2.17×10-7 mol/L的TFA作用时,其UV-Vis光谱发生明显变化,而与7.0×10-10 mol/L的TFA作用时,其荧光光谱强度明显变弱。
| [1] | 麦麦提依明·马合木提, 司马义·努尔拉, 吐尼莎古丽·阿吾提, 等. 二噻吩基喹喔啉的溶液聚合及其酸致变色性能[J]. 功能高分子学报, 2015, 28(3): 242–249. |
| [2] | 贾美琳, 陈庆, 蒋宛莉, 等. 喹啉盐与吡啶盐花青染料分子酸致变色行为的研究[J]. 信息记录材料, 2009, 10(5): 13–16. |
| [3] | 周天佑, 孟宪柱, 唐倩, 等. 光和pH响应的功能单体的合成与表征[J]. 功能高分子学报, 2009, 22(3): 237–252. |
| [4] | PENG Banghua, LIU Guangfei, LANG Liu, et al. Photochromism in solid state and acidichromism in solution of 1-phenyl-3-methyl-4-(4'-methylbenzal)-pyrazolone-5 thiosemicarbazone[J]. Journal of Photochemistry and Photobiology A:Chemistry, 2005, 171(3): 243–249. DOI:10.1016/j.jphotochem.2004.10.011 |
| [5] | LIN Ching-Tsan, SHIH Jen-Hao, CHEN Chung-Ling, et al. Synthesis of novel triketone-based acidichromic colorants[J]. Tetrahedron Letters, 2005, 46(30): 5033–5037. DOI:10.1016/j.tetlet.2005.05.070 |
| [6] | YIN Meifang, JIAO Tifeng, LIU Minghua. Acidichromism in the LB film of bolaform Schiff base[J]. Chinese Chemical Letters, 2007, 18(1): 30–32. DOI:10.1016/j.cclet.2006.11.008 |
| [7] | NIU Haijun, LUO Peihui, ZHANG Milin, et al. Multifunctional, photochromic, acidichromic, electrochromic molecular switch:Novel aromatic poly(azomehine)s containing triphenylamine group[J]. European Polymer Journal, 2009, 45(11): 3058–3071. DOI:10.1016/j.eurpolymj.2009.08.017 |
| [8] | 刘杰, 彭辉, 王海江, 等. pH敏感超支化聚合物的合成与表征[J]. 功能高分子学报, 2010, 23(2): 176–180. |
| [9] | ZHOU Qingqing, ZHANG Xianzhe, LIU Hewen. Synthesis and pH-responsive chromism of a macrocyclic compound with three spiropyran units[J]. Chinese Journal of Applied Chemistry, 2012, 26(12): 1371–1380. |
| [10] | KOCAK G, TUNCER C, BVTVN V. pH-Responsive polymers[J]. Polymer Chemistry, 2017, 8(1): 144–176. DOI:10.1039/C6PY01872F |
| [11] | 再吐尼古丽·库尔班, 木合塔尔·依米提, 帕提古丽·依明, 等. 含偶氮苯与噻吩结构单元的共轭聚合物合成及酸致变色性质[J]. 高分子学报, 2007(12): 1105–1110. DOI:10.3321/j.issn:1000-3304.2007.12.001 |
| [12] | XIRALI Mamtimin, AIERKEN Aikebaierjiang, MUSITAKE Alifujiang, et al. Synthesis, characterization and acidochromism of poly (2-N, N-dimethylamino-4, 6-bis (2-thienyl)-pyrimidine)[J]. Journal of Polymer Research, 2010, 18(1): 105–109. |
| [13] | 赛亚尔·斯迪克, 希尔艾力·买买提依明, 司马义·努尔拉, 等. 含嘧啶与芴结构单元共聚物的合成及性能[J]. 功能高分子学报, 2014, 27(2): 207–212. |
| [14] | 麦麦提依明·马合木提. 含氮缺电子共轭高分子的合成及光、电化学性能研究[D]. 乌鲁木齐: 新疆大学, 2014. |
| [15] | HAO Zengshuai, LI Minjie, LIN Haixia, et al. Synthesis, optical, and electrochemical properties of 2, 3-diphenyl-10H-indeno[1, 2-g]quinoxaline, 15H-dibenzo[a, c]indeno[1, 2-i]phenazine, and 15H-indeno[1, 2-i]phenanthro[4, 5-abc]phenazine derivatives[J]. Dyes and Pigments, 2014, 109: 54–66. DOI:10.1016/j.dyepig.2014.04.042 |
| [16] | LEE Ji Won, SON Ye Seul, LEE Jung Yean, et al. pH-sensitive fluorescent deoxyuridines labeled with 2-aminofluorene derivatives[J]. Tetrahedron, 2016, 72(36): 5595–5601. DOI:10.1016/j.tet.2016.07.049 |
| [17] | HÜSNÜYE Ardıç Alidaǧı, FERDA Hacıvelioǧlu, SÜREYYA Oǧuz Tümay, et al. Synthesis and spectral properties of fluorene substituted cyclic and polymeric phosphazenes[J]. Inorganica Chimica Acta, 2017, 457: 95–102. DOI:10.1016/j.ica.2016.12.013 |
| [18] | KIM Min Ji, LEE Chil Won, GONG Myoung Seon. Deep blue organic light-emitting diode using non anthracene-type fused-ring spiro[benzotetraphene-fluorene] with aromatic wings[J]. Organic Electronics, 2014, 15(11): 2922–2931. DOI:10.1016/j.orgel.2014.08.030 |
| [19] | GUO Wen, ENGELMAN B J, HAYWOOD T L, et al. Dual fluorescence and electrochemical detection of the organophosphorus pesticides-Ethion, malathion and fenthion[J]. Talanta, 2011, 87: 276–283. DOI:10.1016/j.talanta.2011.10.015 |
| [20] | CHAKKOOTH V B B, SOICHIRO O, MASAYUKI T. Oligofluorene-based nanoparticles in aqueous medium:Hydrogen bond assisted modulation of functional properties and color tunable FRET emission[J]. Journal of Materials Chemistry, 2012, 22(22): 11224–11234. DOI:10.1039/c2jm30315a |
 2017, Vol. 30
2017, Vol. 30


